b. Jumlah ikatan
Ikatan kovalen rangkap satu : 2
Ikatan kovalen rangkap dua : 2
Ikatan kovalen koordinasi : 2
Penjelasan:
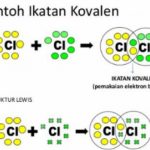
Ikatan Kovalen
Pada ikatan kovalen, pasangan elektron yang digunakan secara bersama dan terletak diantara dua inti atom akan ditarik oleh kedua inti atom yang berikatan. Hal ini akan mempengaruhi distribusi kepadatan elektron antara kedua inti yang berikatan. Kemampuan untuk menarik elektron kearah inti, didasarkan pada sifat keelektronegatifan dari masing-masing unsur yang berikatan.
- Ikatan kovalen polar, merupakan ikatan yang terjadi karena perbedaan keelektronegatian hari masing – masing atom yang berikatan. Secara sederhana dapat dijelaskan dimana kerapatan electron yang membentuk ikatan akan cenderung untuk mengarah ke salah satu atom.
- Kovalen murni (non polar),molekul pembentukuya tidak terjadi momen dipol atau muatan ikatan elektron mendapat gaya tarik yang sama
Macam – Macam Ikatan Kovalen
- Ikatan Kovalen rangkap Satu
Contoh molekul : CH₄, H-Cl
- Ikatan Kovalen rangkap dua
Contoh molekul : C₂H₄ ; O₂, CO₂, SO₂
- Ikatan Kovalen rangkap tiga
Contoh molekul : N₂
Baca juga: Mengenal Asam Karboksilat, Tata Nama dan Sifat-Sifatnya
Baca juga: Reaksi Hidrokarbon, Subtitusi, Adisi dan Eliminasi
Nah, itu dia pembahasan mengenai materi struktur Lewis pada asam sulfat. Semoga materi kali ini dapat bermanfaat ya.