Persamaan Reaksi Kimia Kelas 10 SMA – Reaksi kimia dapat dikatakan sebagai suatu proses yang menggambarkan sebuah zat yang mengalami perubahan. Perubahan ini terjadi akibat reaksi kimia yang dialaminya dan menunjukkan perubahan pada zat-zatnya. Gambaran zat yang terlibat pada proses kimia sering ditemui dalam kehidupan sehari-hari, baik itu perubahan yang menguntungkan atau yang merugikan.
Persamaan kimia dapat dimaknai sebagai sebuah persamaan dasar sebelum melangkah lebih jauh ke persamaan laju reaksi atau persamaan reaksi redoks. Reaksi kimia menjadi suatu proses ketika satu atau lebih zat diubah menjadi suatu zat yang berbeda dan menghasilkan produk yang baru. Suatu persamaan reaksi kimia dapat ditulis dengan dua cara, yaitu persamaan perkataan dan persamaan simbol.
Baca Juga: Pembahasan dan Cara Menentukan Pereaksi Pembatas
Baca Juga: Zat Makanan dengan Energi Tertinggi Pada Satuan yang Sama
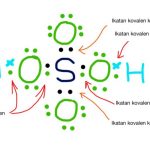
Baca Juga: Struktur Lewis Asam Sulfat H2SO4
Pada kesempatan kali ini kalian akan mempelajari mengenai persamaan reaksi kimia dan beberapa contoh soalnya. Berikut pembahasannya.
Konsep persamaan Reaksi Kimia
Persamaan reaksi kimia dapat dimaknai sebagai sebuah proses yang didasari rumus kimia. Persamaan reaksi kimia dapat memberikan informasi dari akibat suatu proses reaksi dari identitas dan kuantitas suatu zat yang terlibat. Keterlibatan zat ini dapat terjadi akibat suatu perubahan yang terjadi atas proses yang terjadi, baik kimia atau fisika. Pada beberapa zat yang terlibat dalam reaksi dapat menjelaskan jumlah zat setelah reaksi dan dinamakan sebagai pereaksi atau reaktan.
Kejadian reaksi kimia pasti melibatkan rumus-rumus kimia. Pada rumus kimia sendiri terdapat indeks yang berupa angka dan ditulis dalam format subscript (berukuran kecil dengan posisi agak ke bawah). Indeks terletak pada sisi kanan simbol unsur atau kelompok atom unsur (gugus). Indeks menyatakan jumlah atom unsur atau kelompok atom unsur. Misalnya, Br2 menunjukkan terdapat 2 atom Br yang saling berikatan dan Fe(NO3)3 menunjukkan terdapat 1 atom Fe, 3 atom N, dan 9 atom O saling berikatan.
Langkah penyetaraan persamaan reaksi kimia
Konsep penyetaraan persamaan reaksi kimia dapat dilakukan dengan jalan mencoba-coba apabila reaksi yang diberikan adalah reaksi sederhana. Namun, pada beberapa reaksi kimia yang kompleks harus memerlukan beberapa langkah umum yang perlu diterapkan. Berikut langkah-langkah dalam melakukan penyetaraan persamaan reaksi kimia.
- Pilihlah satu rumus kimia yang paling rumit, tetapkan koefisiennya sama dengan 1.
- Zat-zat yang lain tetapkan koefisien sementara dengan huruf.
- Setarakan dahulu unsur yang terkait langsung dengan zat yang tadi diberi koefisien 1.
- Setarakan unsur lainnya dan biasanya akan membantu jika atom O (oksigen) disetarakan paling akhir.
Penjelasan:
Hukum Lavoisier atau Hukum Kekekalan Massa menyatakan bahwa “massa sebelum dan sesudah reaksi adalah sama.”
Massa suatu zat berbanding lurus dengan jumlah atom di dalamnya. Dengan demikian, dapat dikatakan bahwa jumlah atom sebelum reaksi sama dengan jumlah atom hasil setelah reaksi.
Untuk memenuhi hukum kekekalan massa, persamaan reaksi harus menyetarakan jumlah atom yang digunakan oleh koefisien reaksi. Persamaan reaksi yang jumlah atomnya sama disebut persamaan reaksi sempurna atau persamaan reaksi seimbang.
Baca Juga: Sifat Besi Secara Kimia dan Secara Fisika
Baca Juga: Tata Nama Alkohol IUPAC dan Trivial
Baca Juga: Mengenal Asam Karboksilat, Tata Nama dan Sifat-Sifatnya
Artinya, saat menulis reaksi kimia, tidak ada atom yang dapat dihilangkan atau ditambahkan. Jumlah atom dalam reaksi, baik di sisi kiri maupun kanan, harus sama, sehingga diperlukan penyetaraan reaksi kimia. Di bawah ini adalah langkah-langkah untuk menyetarakan reaksi dengan membuat persamaan matematika:
– Memberikan koefisien reaksi yang dinyatakan dengan variabel (misalnya a, b, c, dan d) pada setiap zat;
– Menyusun persamaan matematis berdasarkan kesamaan jumlah atom unsur yang sama di ruas kiri maupun kanan, dengan jumlah atom = koefisien x indeks; dan
– Menyelesaikan persamaan-persamaan matematis yang diperoleh dari langkah 2 dengan terlebih dahulu menetapkan koefisien salah satu zat sama dengan 1. Zat yang dipilih biasanya adalah zat dengan rumus kimia paling kompleks.
Contoh soal
Contoh 1.
Tuliskan dan setarakan persamaan reaksi antara gas metana (CH4) dengan gas oksiden membentuk gas karbon dioksida dan uap air.
Pembahasan:
Langkah 1, Menuliskan rumus kimia dan persamaan reaksi
CH4(g) + O2(g) → CO2(g) + H2O(l)
Langkah 2, Penyetaraan:
– Tetapkan koefisien CH4 = 1, sedangkan koefisien zat-zat lainnya dimisalkan dengan huruf atau variabel.
1 CH4(g) + a O2(g) → b CO2(g) + c H2O(l)
– Setarakan jumlah atom C dan H.
| Jumlah atom di ruas kiri | Jumlah atom di ruas kanan | Σ Ruas Kiri = Σ Ruas Kanan |
| C = 1 | C = b | b = 1 |
| H = 4 | H = 2c | 2c = 4 maka c = 2 |
– Masukkan koefisien b dan c sehingga persamaan reaksi menjadi:
1 CH4(g) + a O2(g) → 1 CO2(g) + 2 H2O(l)