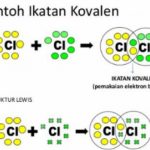
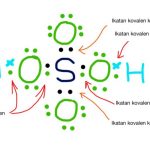
Persamaan kimia menggunakan simbol dan rumus untuk unsur atau senyawa yang terlibat dalam reaksi. Persamaan kimia menggambarkan reaksi reaktan ke produk yang ditunjukkan oleh panah. Koefisien stoikiometri ditempatkan sebelum simbol atau rumus dalam persamaan untuk menyetarakan persamaan. Menurut hukum kekekalan massa, setiap unsur pada sisi produk memiliki kuantitas yang sama seperti pada sisi reaktan.
8. Stoikiometri Reaksi
Stoikiometri melibatkan hubungan kuantitatif dalam reaksi kimia. Faktor stoikiometri, juga dikenal sebagai rasio mol, didasarkan pada koefisien dalam persamaan setara dan digunakan untuk menghubungkan reaktan atau produk. Massa molar dan faktor stoikiometri digunakan untuk memberikan informasi tentang salah satu reaktan atau produk dalam reaksi kimia. Strategi perhitungan stoikiometri reaksi dapat digambarkan pada diagram di bawah ini.
Baca Juga: Sifat Besi Secara Kimia dan Secara Fisika
Baca Juga: Gambar Tabel Periodik dan Cara Membacanya
9. Pereksi Pembatas
Pereaksi pembatas dalah pereaksi yang benar-benar habis digunakan dalam reaksi. Jumlah teoritis produk yang terbentuk dapat ditentukan dari pereaksi pembatas. Pereaksi yang lain disebut pereaksi berlebih. Dalam stoikiometri, pereaksi pembatas harus ditentukan terlebih dahulu.
10. Persen Hasil
Secara teoritis dihitung dari pereaksi. Jumlah yang diperoleh dari reaksi kimia, yang disebut hasil percobaan, seringkali lebih kecil dan umumnya dinyatakan sebagai persentase hasil teoritis.
11. Larutan dan Stoikiometri Larutan
Larutan dibuat dengan melarutkan zat terlarut dalam pelarut. Zat terlarut biasanya hadir dalam jumlah yang sedikit lebih kecil. Molaritas (M) atau konsentrasi molar suatu larutan adalah jumlah mol zat terlarut per liter larutan.
Pengenceran adalah peningkatan volume pelarut. Tetapi jumlah zat terlarut tidak berubah. jadi konsentrasinya menurun. Perhitungan reaksi stoikiometri dalam larutan sering menggunakan molaritas sebagai faktor konversi.
Itu dia pembahasan singkat mengenai konsep-konsep dasar yang mempelajari ilmu stoikiometri. Pahami dengan baik materi kali ini supaya kamu bisa mempelajari materi-materi selanjutnya dengan baik.