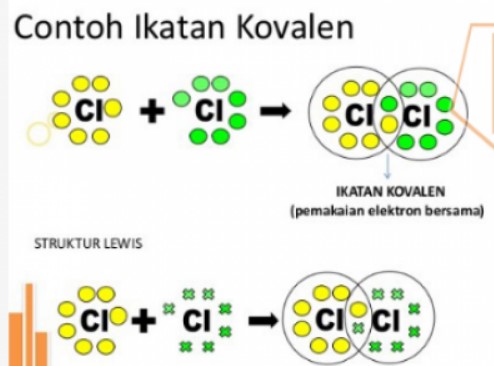
Atom-atom yang terlibat dalam ikatan kovalen adalah atom-atom non-logam. Ikatan kovalen memiliki sifat-sifat sebagai berikut.
– Sebagian besar mudah menguap.
– Memiliki titik didih dan leleh yang rendah.
– Tidak larut dalam air, tetapi larut dalam larutan organik.
– Pada umumnya tidak menghantarkan listrik.
– Berupa gas, cairan atau padatan lunak pada suhu ruang.
– Keadaan murni bersifat isolator.
Baca juga: Materi Eksponen Matematika Kelas 10
Baca juga: Pelayangan Bunyi Rumus dan Contoh Soal
Pembagian Jenis Ikatan Kovalen
Ikatan kovalen dibagi menjadi tiga bagian yang terdiri atas ikatan kovalen tunggal, rangkap dua, dan rangkap tiga. Berikut pembahasannya.
1. Ikatan Kovalen Tunggal
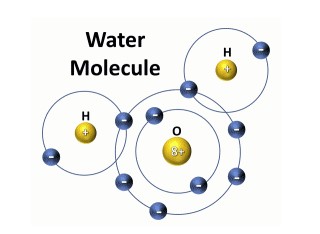
Molekul air termasuk contoh ikatan kovalen tunggal (sumber gambar: serc.carleton.edu)
Ikatan kovalen tunggal adalah ikatan yang terjadi antara dua atom yang membentuk ikatan dengan satu pasang elektron yang digunakan secara bersama. Misalnya, ikatan antara 17Cl dengan 17Cl pada molekul Cl2. Konfigurasi elektron 17Cl = 2, 8, 7. Jumlah elektron valensi atom Cl adalah 7, berarto atom Cl membutuhkan 1 elektron untuk mencapai kestabilan (oktet).
2. Ikatan Kovalen Rangkap Dua
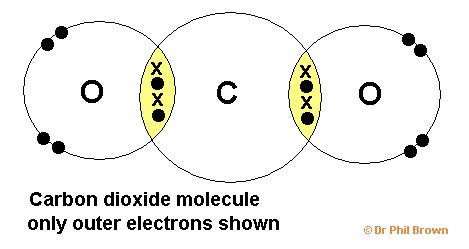
Molekul karbon dioksida termasuk dalam ikatan kovalen rangkap dua
Ikatan kovalen rangkap dua adalah ikatan yang terjadi antara dua atom yang membentuk ikatan dengan dua pasang elektron yang digunakan secara bersama. Misalnya, ikatan antara 😯 dengan 😯 pada molekul O2. Konfigurasi elektron 😯 = 2, 6. Jumlah elektron valensi atom O adalah 6, berarti atom O membutuhkan 2 elektron untuk mencapai kestabilan (oktet).
3. Ikatan Kovalen Rangkap Tiga
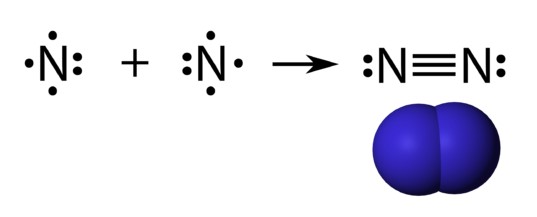
Contoh ikatan kovalen rangkap 3 (sumber gambar: courses.lumenlearning.com)
Ikatan kovalen rangkap tiga adalah ikatan yang terjadi antara dua atom yang membentuk ikatan dengan tiga pasang elektron yang digunakan secara bersama. Misalnya, ikatan antara 7N dengan 7N pada molekul N2. Konfigurasi elektron 7N = 2,5. Jumlah elektron valensi atom N adalah 5, berarti atom N membutuhkan 3 elektron untuk mencapai kestabilan (oktet).